Zusammenfassung
- Mit Hilfe des im HSA KIT automatisch erstellten Balkendiagramms können Gruppen hinsichtlich der Anzahl der gH2AX-Signale unter verschiedenen Bedingungen (z. B. Inkubationsdauer einer bestimmten Substanz, Intensität einer Substanz, Alter der Tiere usw.) verglichen werden. Darüber hinaus kann die Gesamtfläche der gH2AX-Signale, aufgetragen gegen die Gesamtfläche des Gewebes, sowohl zwischen den Gruppen als auch innerhalb jeder Gruppe verglichen werden.
- Hohe Werte für Genauigkeit (= 0,962), Präzision (= 0,966), Wiedererkennung (= 0,995) und F1-Score (= 0,980)
- Viele Anwendungsfälle:
- Verbesserung neuer Medikamente gegen Tumore wie ProstatakrebsVerbesserung
- neuer Medikamente zum Schutz von Organen wie der Niere
Die Radioligandentherapie zielt auf die selektive Eliminierung von Tumorzellen durch fokussierte Strahlung ab. Dennoch ergeben sich im Zusammenhang mit der Radionuklidtherapie zusätzliche therapeutische Optionen. Eine vielversprechende Strategie ist die mögliche Kombination der Radionuklidtherapie mit dem Einsatz von Protektoren zur Krebsbehandlung. Dieser Ansatz erweist sich als besonders relevant, da die verabreichte Strahlung auch das umliegende Gewebe beeinträchtigen kann. Wird zum Beispiel der Tumor in der Niere bestrahlt, wird auch das umliegende gesunde Nierengewebe zerstört. Um die unerwünschten Auswirkungen auf das gesunde Gewebe zu minimieren, könnte vor der Strahlentherapie der Einsatz von Schutzsubstanzen erwogen werden. Im Folgenden wird erläutert, wie ein solcher Versuch im Kern aussehen könnte und wie er durch das HSA KIT effizient unterstützt wird.
gH2Ax-Signale
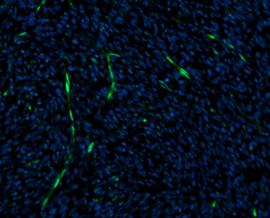
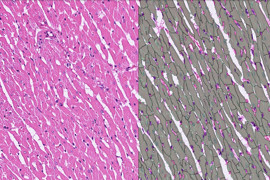
Intra- und extrazelluläre Einflüsse, wie z.B. radioaktive Strahlung bei der Radioimmuntherapie, können Mutationen oder DNA-Doppelstrangbrüche (DSBs) verursachen. Nach der Induktion von DSBs kommt es innerhalb weniger Minuten zur Phosphorylierung der Histon H2A-Variante H2AX (gH2AX). Sie kann eine potenzielle Gefahr für die Zelle und damit für den gesamten Organismus darstellen. Je nach Ausmaß der Schädigung kann der programmierte Zelltod (Apoptose) ausgelöst werden oder die Zelle kann nekrotisieren. Aus diesem Grund suchen Labore nach einer Substanz zum Schutz von Nebenorganen während einer Radioimmuntherapie. Zur Überprüfung der Wirkung dieser kann der „gH2AX Analyzer“ im HSA KIT verwendet werden, um die gH2AX-Signale zu quantifizieren, die mit den DSBs korrelieren.
Vorteile des HSA KIT
- Evidenzbasierte Entwicklung: Das HSA KIT basiert auf Erkenntnissen aus Experimenten. Die Projekte werden archiviert, so dass die Daten auch nach 2 Jahren noch nachvollziehbar sind. Damit ist sichergestellt, dass die verwendeten Einstellungen und Parameter auch nach längerer Zeit noch nachvollzogen werden können.
- Einfache Modifikation: Das Ändern von Experimenten wird durch die Copy-Tool-Funktion des HSA KIT vereinfacht. Es ermöglicht das schnelle Kopieren von Projekten unter Beibehaltung der bisherigen Daten. Es wird ein neues Projekt mit einer neuen IP erstellt, wobei sichergestellt wird, dass keine früheren Daten verloren gehen. Anschließend können neue Verarbeitungen und Parameteranpassungen vorgenommen werden, was einen einfachen Vergleich der Daten und eine mögliche Auswertung erleichtert.
Diese Funktionen des HSA KIT verbessern die Rückverfolgbarkeit der Daten, ermöglichen effiziente Änderungen und erleichtern die effektive Auswertung der Versuchsergebnisse.
Anwendungsfälle
- Mit dem HSA KIT können die Auswirkungen unterschiedlicher Substanzen, Substanzkonzentrationen, Inkubationszeiten, Strahlungsintensitäten, Mehrfachverabreichungen und ähnlicher Faktoren auf die Intensität der Schädigung bewertet werden.
- Neoadjuvante Therapien können ebenso untersucht werden wie verschiedene Radioisotope wie der Alpha-Strahler Actinium-225 oder der Beta-Strahler Lutetium-177.
- Die Effizienz von zielgerichteten Radiopharmaka kann relativ einfach, schnell und umfassend untersucht werden.
- Es kann eine Aussage darüber getroffen werden, welche Antikörper-Wirkstoff-Konjugate wie viel Wirksamkeit zeigen.
- Das Modell ist so empfindlich, dass es sowohl auf die Niere, die Leber als auch auf Tumore angewendet werden kann.
- Das im HSA KIT automatisch erstellte Balkendiagramm ermöglicht den Vergleich von Gruppen anhand der Anzahl der gH2AX-Signale unter verschiedenen Bedingungen (z. B. Inkubationsdauer einer bestimmten Substanz, Intensität der Substanz, Alter der Tiere usw.). Darüber hinaus kann die Gesamtfläche der gH2AX-Signale, die der Gesamtfläche des Gewebes gegenübergestellt wird, sowohl zwischen verschiedenen Gruppen als auch innerhalb jeder spezifischen Gruppe verglichen werden.
Klicken Sie hier, um einen Blog über ein reales Experiment mit dem HSA KIT zu lesen:
gH2AX-Analysator für die pharmazeutische Forschung
Implementierung und Schulung
Das HSA KIT kann digital erzeugte Mikroskopiebilder von Diascannern (wie dem Axio Scan Z.1) erkennen und analysieren. Dies umfasst die Unterstützung von Bildformaten wie .tiff, .czi und .jpg.
Um die Erkennung von gH2AX-Signalen zu optimieren, wurden zwei Deep-Learning-Modelle trainiert. Das erste Modell mit der Bezeichnung „HyperNonVesselNet“ ist für die Erkennung von Erythrozyten und Blutgefäßen konzipiert. Es unterteilt die gesamte Niere in Nicht-Gefäß- und Gefäßbereiche. Ziel ist es, die relevanten Bereiche oder Objekte in einem Bild zu identifizieren und sie vom Hintergrund und/oder anderen Objekten zu trennen.
Das zweite Modell, „HypergH2AXNet“, wird als Unterstruktur innerhalb des Nicht-Gefäßbereichs angewendet.
Die für das Training des Deep-Learning-Modells verwendeten Ground-Truth-Daten (GTD) wurden mit der HSA KIT-Software erstellt.
Das Modell „HypergH2AXNet“ wurde für die Quantifizierung von gH2AX-Signalen trainiert. Der Trainingsprozess war zeitaufwändig und umfasste mehrere Optimierungsansätze, die berücksichtigt, ausgeführt und die Ergebnisse überprüft wurden.
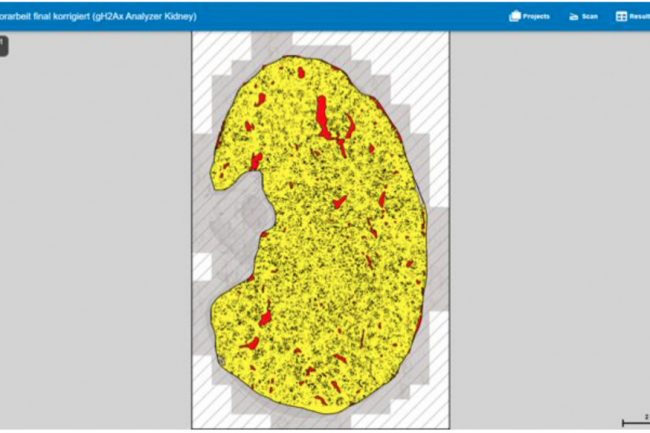
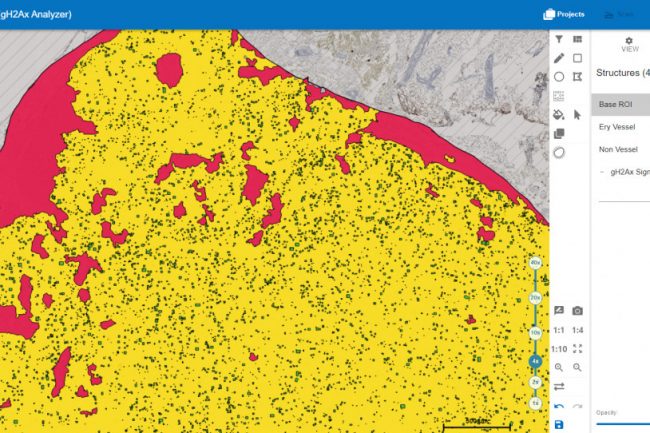
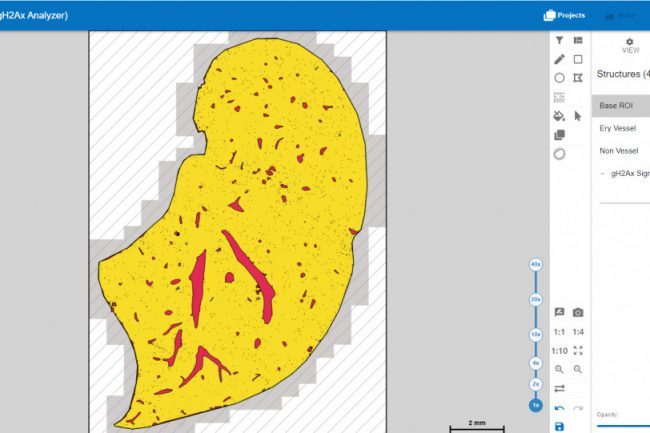
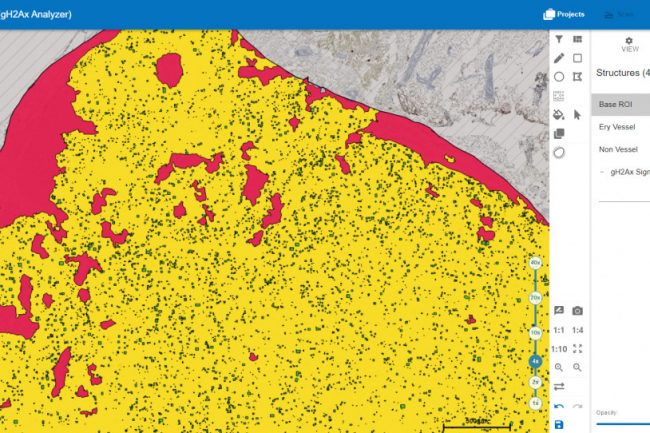
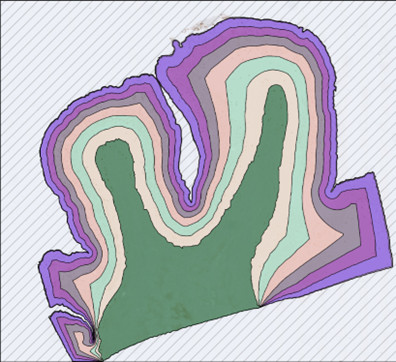
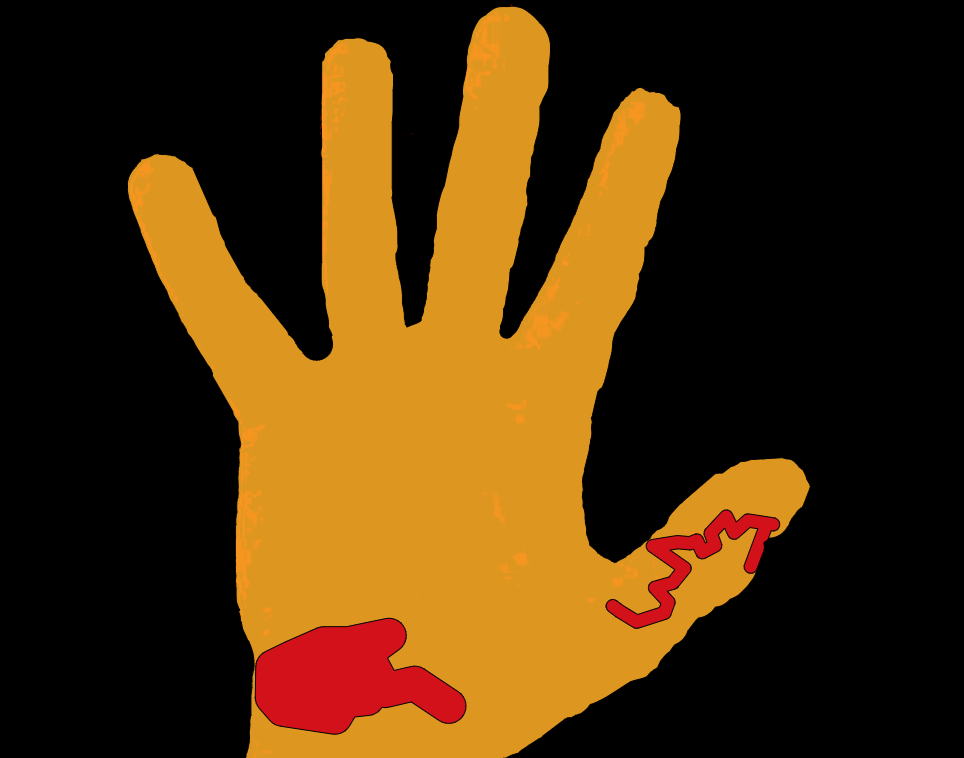
Die folgende Abbildung zeigt eine Niere, die mit dem HSA KIT quantifiziert wurde. Die gelbe Struktur stellt die Nicht-Gefäße dar, die roten Strukturen die Erythrozyten und Blutgefäße, die schwarzen Strukturen die gH2AX-Signale.
Signaldetektion mit dem HSA KIT in der Mausniere
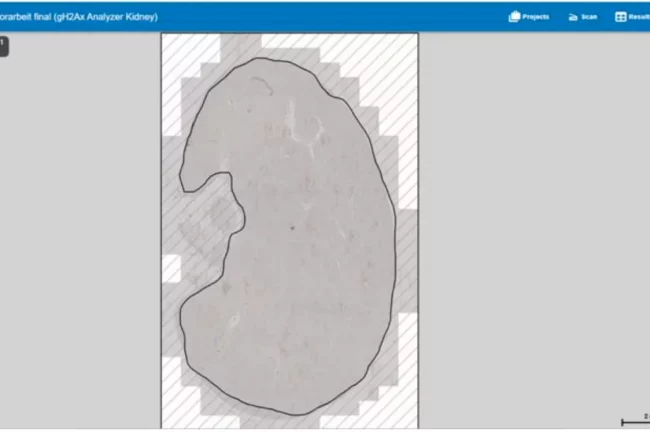
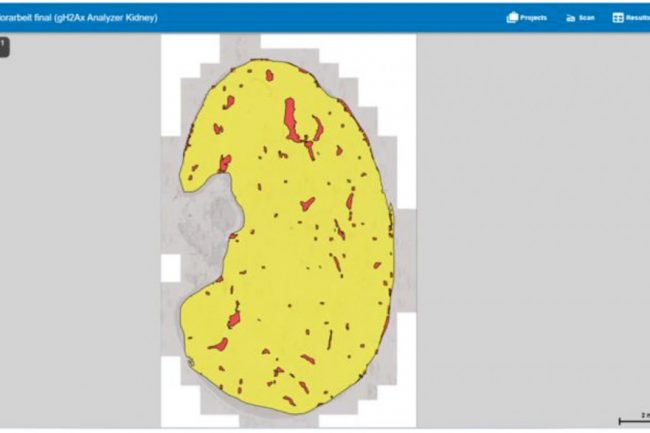
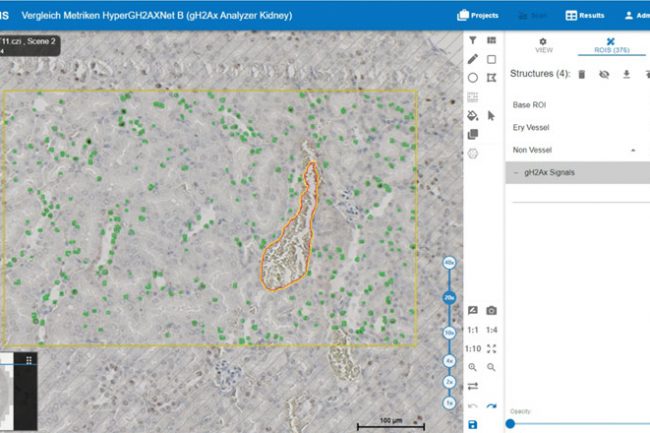
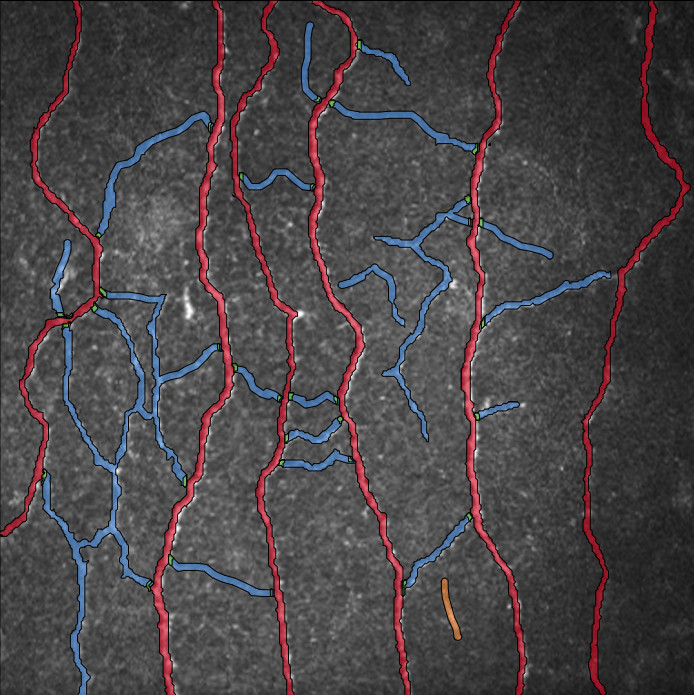
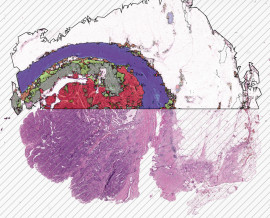
Um die Plausibilität der Software-Ergebnisse zu überprüfen, wurden die Schnitte einzeln untersucht. Dabei wurden alle vom HSA KIT automatisch identifizierten Strukturen berücksichtigt, einschließlich des Nicht-Gefäßbereichs, der Erythrozyten oder Gefäße und der gH2AX-Signale. Zunächst wurde die gesamte Niere untersucht, um größere Fehler auszuschließen. Anschließend wurden am Beispiel einer Mäuseniere die dargestellten und verborgenen Strukturen verglichen.
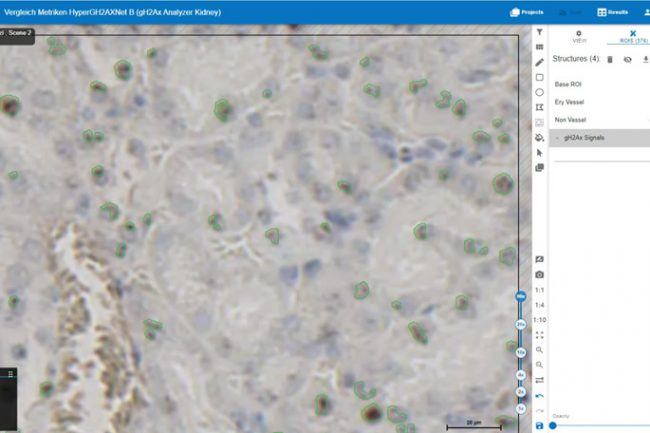
Die bereits erwähnte Basis-ROI (Region of Interest) wird durch den schwarzen Umriss der Niere dargestellt. Damit wird der zu quantifizierende Bereich definiert, und alle erkannten und analysierten Signale befinden sich innerhalb dieser Markierung. Der Bereich außerhalb dieser Markierung ist mit schwarzen diagonalen Linien gefüllt, was bedeutet, dass dieser Bereich von der Quantifizierung ausgeschlossen ist. Die rot markierten Strukturen stellen Erythrozyten oder Gefäße dar. Dank der automatischen Erkennung dieser Strukturen muss der Ausschluss von Blutgefäßen und roten Blutkörperchen nicht manuell vorgenommen werden. Dies ermöglicht die Definition des Nicht-Gefäß-Bereichs, der in gelb dargestellt ist. Innerhalb dieses Bereichs werden die gH2AX-Signale quantifiziert, dargestellt in Schwarz. Für die Ergebnisberechnung dient der Nicht-Gefäßbereich als Basis für die gesamte Niere, da er nur Zellen enthält, in denen potenzielle DNA-Schäden auftreten können.
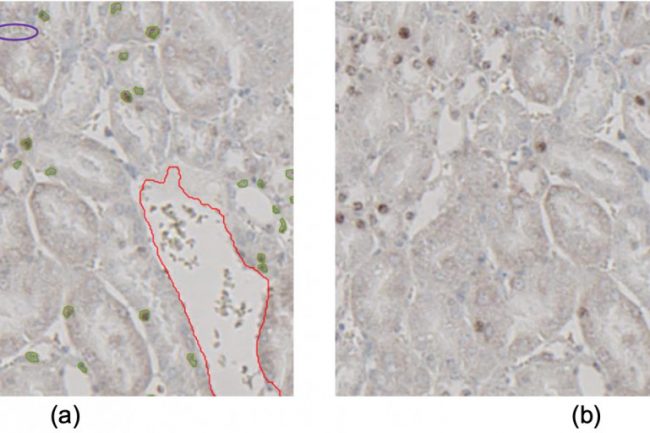
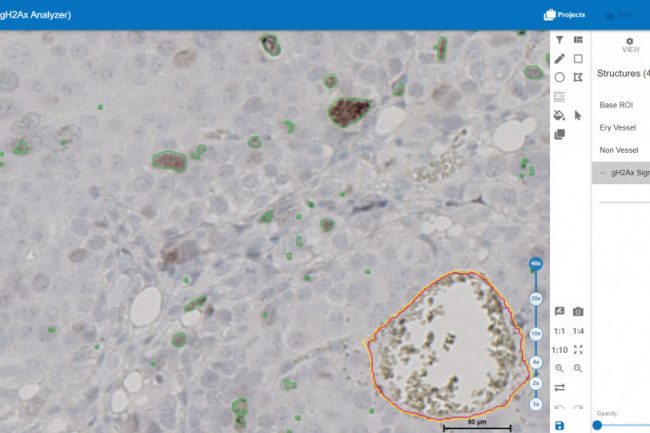
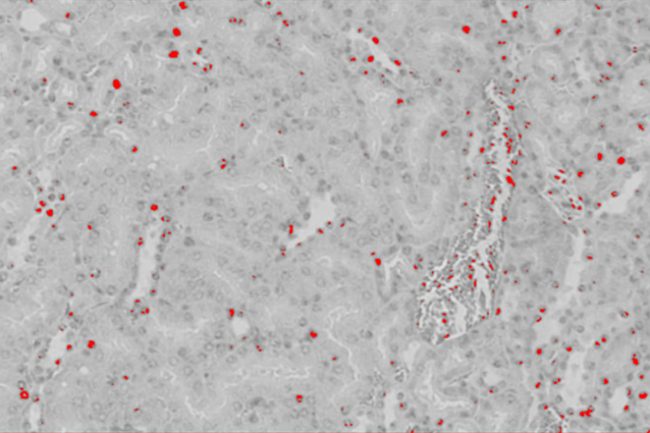
Um die Qualität der Ergebnisse zu bewerten, werden außerdem die als Signale erkannten Färbungen ein- und ausgeblendet und untersucht. Letzteres geschah, um einen besseren Vergleich zu ermöglichen und festzustellen, ob diese Stellen Signale darstellen oder nicht. Die Bildausschnitte wurden bei 40-facher Vergrößerung im HSA KIT aufgenommen und später im Verlauf der Studie verglichen.
Die als Signale erkannten Strukturen sind in Abbildung Xa grün hervorgehoben. Der rot markierte Bereich wurde von der Software als Erythrozyt identifiziert. Der Nicht-Gefäßbereich, der normalerweise in Gelb erscheint, wurde in beiden Bildausschnitten zur besseren Übersicht ausgeblendet. Es ist zu beobachten, dass innerhalb der Erythrozyten keine Signale zu erkennen sind. So sind zum Beispiel die roten Blutkörperchen im Bild lila eingekreist. Diese Strukturen zeichnen sich durch einen Hohlraum aus, der mit gelblichen, unregelmäßigen Strukturen gefüllt ist. Sowohl die Hohlräume als auch die Strukturen darin können in Größe und Form variieren. Das Modell wurde so trainiert, dass es nur größere Blutgefäße und Blutzellen (>100 μm) erkennt, da kleinere Blutgefäße und Blutzellen oft zwischen den Zellen vorhanden sind (lila) und keinen negativen Einfluss auf die Qualität der Ergebnisse haben, da das Modell sie nicht fälschlicherweise als positiv erkennt. Weitere Einzelheiten hierzu und zum Trainingsverfahren wurden im Abschnitt „Training“ erläutert. Wie im Bildausschnitt zu sehen ist, wurden diese Strukturen nicht als Signale erkannt. Außerdem wurden in diesem Bildausschnitt keine Strukturen fälschlicherweise als gH2AX-Signale identifiziert, was darauf hindeutet, dass an dieser Stelle keine falsch-positiven Ergebnisse erzeugt wurden. Außerdem zeigt der Bildausschnitt, dass kein falsch-negatives Signal erkannt wurde. Jedes eindeutige Signal, unabhängig von seiner Größe, in Abbildung a wurde von der Software korrekt erkannt. Daher liegt die Fehlerquote an dieser Stelle bei 0 % sowohl für falsch-positive als auch für falsch-negative Signale.
Erkennung im Tumor
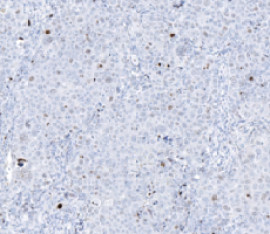
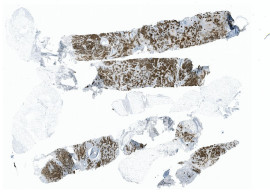
Das Modell kann auch zum Nachweis von gH2AX-Signalen in anderen Geweben und Organen verwendet werden. Im folgenden Abschnitt wird die Bewertung eines Tumors mit Hilfe des HSA KIT beschrieben.
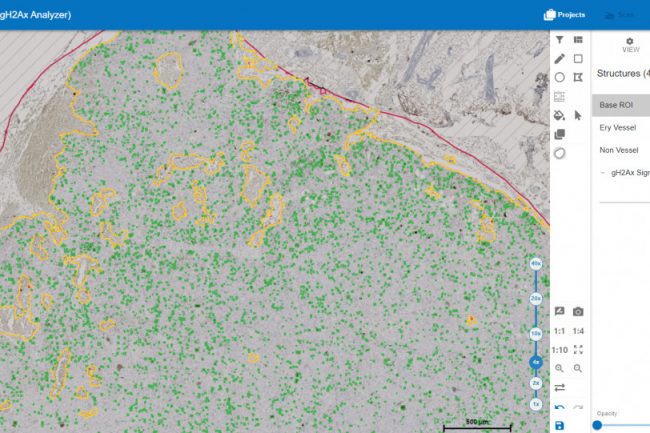
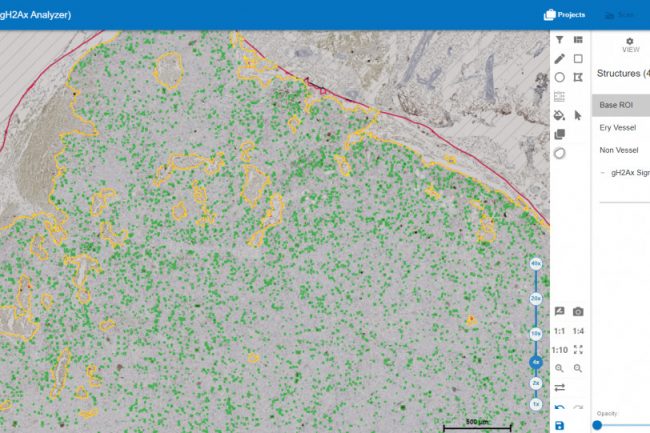
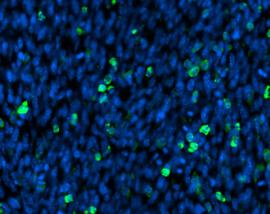
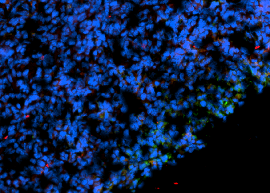
Es ist offensichtlich, dass die Blutgefäße und die roten Blutkörperchen (Erythrozyten) als solche erkannt wurden (in rot). Der Rest des Tumors, in dem Zellkerne und damit DNA-Doppelstrangbrüche vorhanden sein könnten, wurde als Nicht-Gefäßbereich erkannt (in gelb). In diesem Bereich wurden DNA-Doppelstrangbrüche in Form von gH2AX-Signalen (in grün) identifiziert.
Die folgenden Auszüge geben einen detaillierteren Einblick in die Signalerkennung.
Auch hier sind die bereits erwähnten Strukturen erkennbar, darunter die Erythrozyten (in rot), der Nicht-Gefäßbereich (in gelb) und die gH2AX-Signale (in grün).
Nachweis in der Leber
Dieser Abschnitt veranschaulicht die Signaldetektion des HSA KIT (Software) in der Leber einer Maus.
Mit dem HSA KIT ist es möglich, gH2AX-Signale nicht nur in der Niere, sondern auch in anderen Geweben, wie Tumoren und der Leber, nachzuweisen. Für einen besseren Überblick wurde im Blog die Anwendung auf die Niere näher betrachtet.
Automated area calculation of the gH2AX signals with the HSA KIT
Die Dateinamen im folgenden Abschnitt wurden fiktiv erstellt und spiegeln nicht die tatsächlichen Ergebnisse des Experiments, sondern den tatsächlichen Ablauf wider.
Die gescannten OTs wurden mit dem HSA KIT analysiert. Die Parameter wurden entsprechend der Färbeintensität optimiert und angepasst, indem verschiedene Einstellungen vorgenommen und überprüft wurden, auf die später noch näher eingegangen wird. Ziel war es, den gesamten Bereich jedes einzelnen Signals zu erfassen und die Erkennung von unspezifischen Färbungen und roten Blutkörperchen zu minimieren.
Durch den Vergleich der Ergebnisse verschiedener Einstellungen wurde ein Konfidenzwert von 0,70 als optimal ermittelt. Dieser Parameter gibt den Grad des Vertrauens der Software in die erkannten Signale an und reicht von 0 bis 1. Zusätzlich wurde ein Bereich von 0 bis 5.000.000 μm2 für den Größenbereich festgelegt, in dem Signale erkannt werden sollten. Da die Bereiche von DNA-Doppelstrangbrüchen stark variieren können, wurde diese Option nicht weiter berücksichtigt.
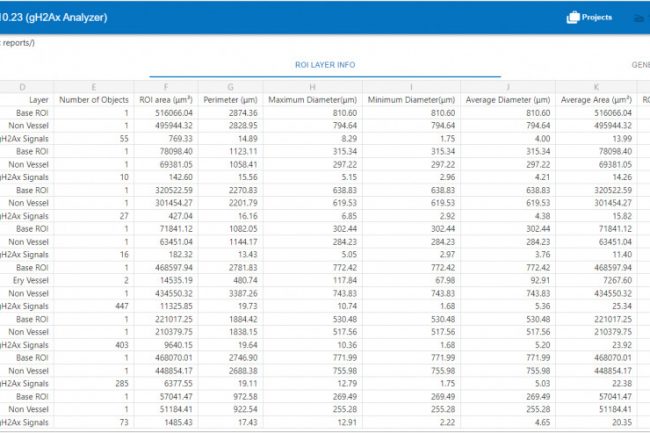
Nach der Optimierung der Parameter wurde das Modell auf die Proben angewendet, und die Fläche der gH2AX-Signale wurde von der Software automatisch berechnet. Die Gesamtflächen der Nieren wurden ebenfalls automatisch berechnet, so dass ein Vergleich zwischen den Gesamtschädigungsflächen und den Nierenflächen möglich ist. Darüber hinaus wurde der prozentuale Anteil der Schäden innerhalb der Dreifachbestimmungen gemittelt und die Standardabweichung berechnet (Tabelle 1).
Zur Visualisierung dieser Werte erstellte das HSA KIT ein Balkendiagramm, das den Prozentsatz der DNA-Schäden im Verhältnis zur Gesamtfläche der Niere darstellt. Es wurden die gemittelten Werte der Schäden von 3 behandelten Tieren pro Gruppe und Zeitpunkt verwendet. Die Standardabweichungen wurden ebenfalls berücksichtigt.
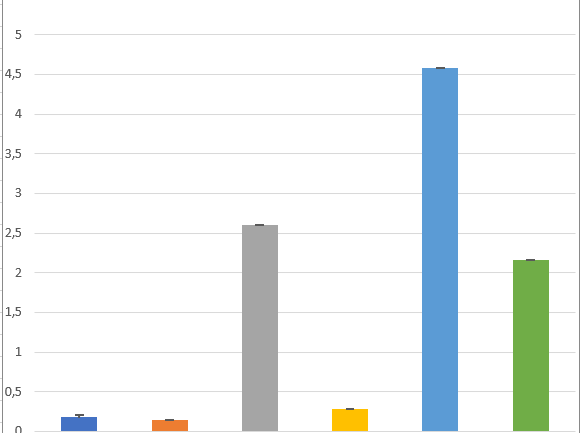
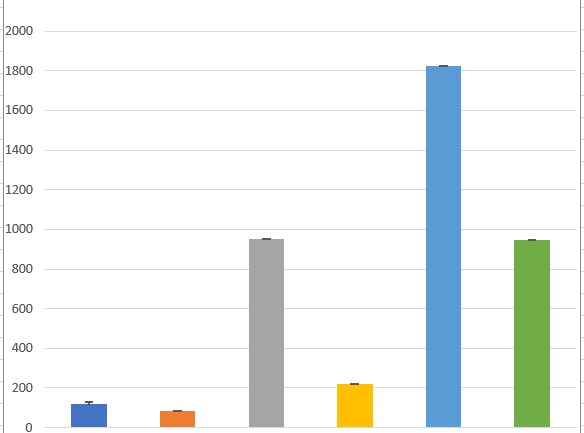
Zusätzlich zur Gesamtfläche der Schädigung im Verhältnis zur Gesamtfläche der Niere erstellt das HSA KIT automatisch ein Säulendiagramm, das die Gesamtzahl der gH2AX-Signale pro mm2 für jedes Tier angibt.
Es ist zu beobachten, dass die Tiere aus Gruppe 1, die nur zwei Stunden lang mit der Substanz bebrütet wurden (dunkelblaue Balken), weniger geschädigt sind. Der Balken mit den 15-Stunden-Werten der Gruppe 1 (orange) zeigt die geringste Schädigung an. Die Tiere der Gruppe 2, die 2 Stunden lang bebrütet wurden (grau), weisen ein ähnliches Ausmaß an Schädigung auf wie Gruppe 3 (grün). Die Gruppe 3, die den höchsten Schaden aufweist, wurde 2 Stunden lang bebrütet (hellblau).
Das Säulendiagramm deutet darauf hin, dass die Gruppenzahl einen Einfluss auf das Ausmaß der DNA-Schäden hat. Wenn die Inkubationszeit konstant bleibt (2h oder 15h) und sich nur die Gruppenzahl ändert, indem die Konzentration der Substanz verändert wird, steigt die Anzahl der Schäden deutlich an.
Die eingefügten Standardabweichungen zeigen kein klares Muster der Zunahme oder Abnahme.
Modelle für die Signalerkennung
Mit dem HSA KIT ist es möglich, bestimmte Parameter je nach Abschnitt einzustellen. Es wurde darauf geachtet, diese Parameter so zu wählen, dass möglichst viele manuell identifizierte γH2AX-Signale automatisch erkannt werden können. Außerdem wurde die gesamte Fläche dieser Signale berücksichtigt, da später in der Studie die Berechnung der Signalfläche vorgesehen war.
Der Recall-Wert des Modells „Hypergh2axNet“ lag bei 0,995 und der Präzisionswert bei 0,966, was bedeutet, dass es mehr falsch-positive Ergebnisse gab (d. h. ein Signal wurde erkannt, obwohl es nicht vorhanden war) als falsch-negative Erkennungen. Dies lässt sich an der Anzahl der falsch-negativen (FN) und falsch-positiven (FP) Ergebnisse ablesen. Allerdings weicht keiner der berechneten Werte signifikant von 1 ab, was darauf hindeutet, dass das Modell für die genaue Quantifizierung von γH2AX-Signalen geeignet ist. Der harmonische Mittelwert, der F1-Score, liegt bei 0,980, was ein weiterer Beleg dafür ist, dass es sich um ein geeignetes Deep-Learning-Modell handelt.
Metriken
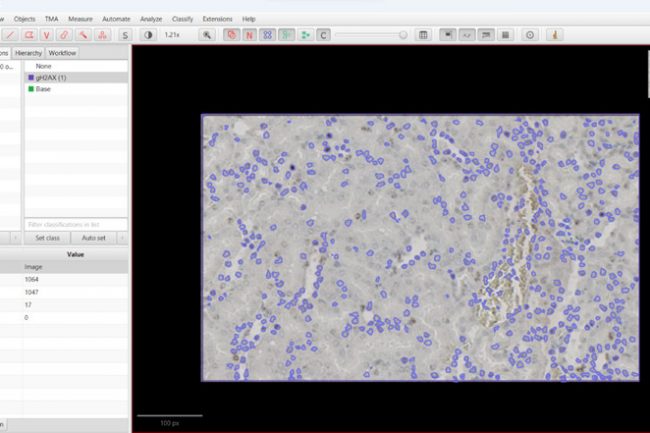
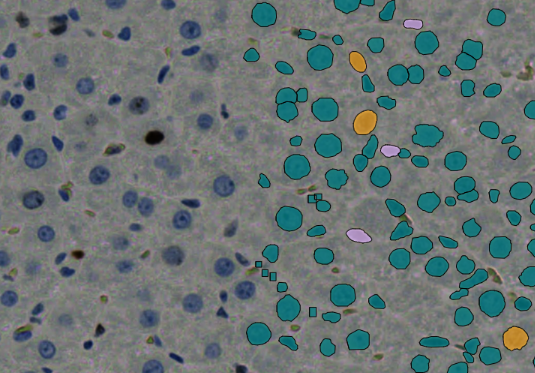
Um die Qualität des Modells weiter zu untersuchen, wurden Metriken berechnet. Zu diesem Zweck wurde eine Region einer Niere ausgewählt und gH2AX-Signale wurden manuell erkannt.
Im nächsten Schritt wurde ein Vergleich mit HSA KIT durchgeführt, um festzustellen, welche manuell annotierten Signale vom Modell automatisch erkannt wurden und welche nicht. Auf dieser Grundlage wurden die Werte für die Anzahl der FN (falsch-negativen), TN (wahr-negativen), FP (falsch-positiven) und TP (wahr-positiven) gezählt.
Die folgenden Werte wurden ermittelt:
FN: 2
TN: unbestimmbar
FP: 15
TP: 432
Anhand dieser Werte und der Gleichungen (1.1) bis (1.4) wurden die Metriken Genauigkeit, Präzision, Wiedererkennung und F1-Score berechnet. Da die TN-Werte unbestimmbar sind, wurden sie nicht weiter berücksichtigt. Die folgenden Werte wurden ermittelt:
Genauigkeit = 0,962
Präzision = 0,966
Rückruf = 0,995
F1-Ergebnis = 0,980
Der Rückruf-Wert ist der höchste unter allen Werten, gefolgt vom F1-Score. Der Präzisionswert ist etwas höher als die Genauigkeit.
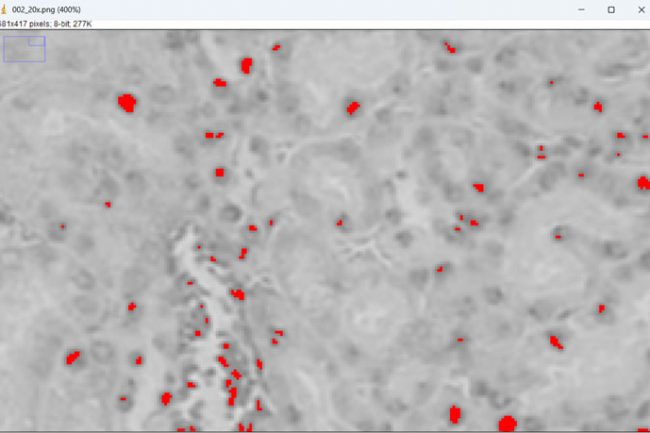
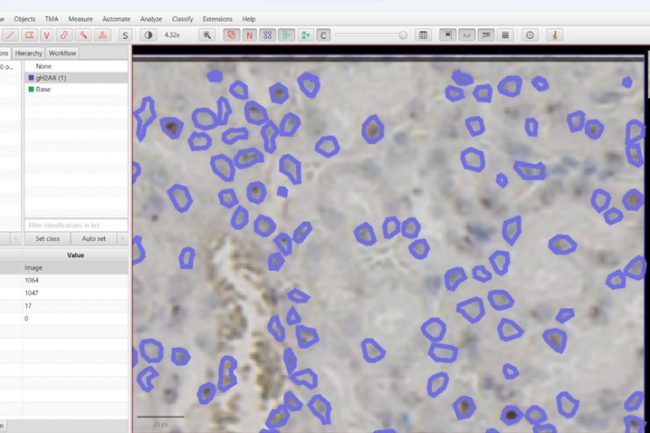
HSA KIT vs. ImageJ vs. QuPath
Um die Ergebnisse besser vergleichen zu können, haben wir einen Zoomfaktor von 80 verwendet.
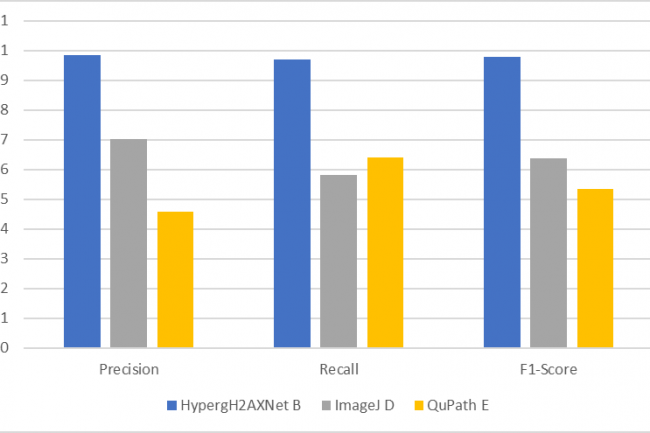
Mit diesen Daten wurde ein Säulendiagramm erstellt, bei dem die blaue Säule für HSA HypergH2AXNet, die schwarze Säule für ImageJ und die letzte (gelbe) für QuPath steht. Die Metriken Präzision, Recall und F1-Score wurden für jede Methode berechnet, um die Methoden besser vergleichen zu können.
Wenn man alle Säulen vergleicht, kann man sehen, dass das Modell „HypergH2AXNet“ die Säule mit dem höchsten Durchschnittswert aller Modelle hat. ImageJ und QuPath befinden sich ungefähr auf dem gleichen Niveau.